Tudományos és műszaki jelentés [II] - 112CI/2017 sz. Projekt
Ez a cikk nincs még lefordítva. Elolvashatod az eredetit Román nyelven az alábbi lapon:
Eredeti cikk

Dezvoltarea unor produse funcționale nutraceutice cu aplicații în alimentația sănătoasă și medicina regenerativă, obținute prin utilizarea unor tehnologii inovatoare și sustenabile.
Faza de execuție Nr. II/2017
Durata proiectului: 24 luni (01/10/2016 - 30/09/2018)
- Caracterizarea proprietăților fizico-chimice ale Zonarului și implementarea unui model in vivo pentru studiul efectelor funcționale nutraceutice ale Zonarului în Diabetul zaharat experimental.
- Studiul proprietăților bioactive ale Zonarului și realizarea a 2 modele in vivo pentru studiul efectelor Zonarului asupra carcinomului de colon C26 și melanomului B16 la animale de laborator.

Obiective generale 28BG/2016
- Caracterizarea proprietăților bioactive și a componentelor fizicio-chimice ale Zonarului, utilizând metodologii de investigație ultramoderne (ex: cromatografia, spectrofotometria);
- Studiul efectelor biologice bioactive ale consumului de Zonar în contextul unor tulburări induse experimental la animale de laborator, comparativ cu animalele sănătoase;
- Investigarea efectelor funcționale și nutraceutice ale Zonarului pe modele de studiu in vitro;
- Sinteza acizilor polilactici utilizând ca sursă accesibilă și avantajoasă economic Zonarul;
- Brevetarea Zonarului ca produs bioactiv nutraceutic cu aplicații în alimentația sănătoasă și medicina regenerativă;
Obiective specifice etapei II/2017
- Determinarea compoziției chimice a Zonarului utilizând metode standardizate clasice;
- Implementarea unui model in vivo pentru studiul efectelor funcționale nutraceutice ale Zonarului într-un model experimental de Diabet zaharat realizat pe șobolani Wistar;
- Determinări cantitative și calitative ale proteinelor și peptidelor bioactive din Zonar;
- Dezvoltarea a 2 modele in vivo pentru evaluarea impactului clinic și paraclinic al consumului de Zonar asupra dezvoltării carcinomului Walker 256 și Ascitei Ehrlich.
Activități desfășurate în etapa II/2017
- Studii analitice și experimentale vizând determinarea și caracterizarea componentelor bioactive din Zonar (PP1);
- Model experimental de Diabet zaharat de tip II realizat pe șobolani Wistar prin administrare de Streptozotocin și Nicotinamină (CO);
- Determinarea cantitativă și calitativă a unor componente biologic active din Zonar (PP1);
- Determinarea tranzițiilor serice și termice ale Zonarului prin utilizarea tehnicii DSC (PP1);
- Evaluarea efectelor funcționale nutraceutice ale Zonarului pe model de carcinom Walker 256 grefat la șobolani Wistar, și pe un model de Ascită Ehrlich inoculată la șoareci Swiss (CO);
- Diseminarea rezultatelor prin participare la manifestări științifice naționale/ internaționale şi publicarea rezultatele obținute în jurnale de specialitate indexate Web of science sau BDI (CO+PP1);
- Actualizarea paginii Web în scopul promovării activităților și rezultatelor cercetării.
Rezumatul etapei II/2017
Etapa II/2017 a proiectului nr. 28BG/2016 (PROFI-ZONAR) a urmărit atingerea unor obiective specifice, constând în:
determinarea compoziției chimice a Zonarului cu ajutorul unor metode clasice standard; studiul efectelor funcționale nutraceutice ale
Zonarului pe un model de Diabet zaharat; determinări cantitative și calitative ale proteinelor bioactive din Zonar;
realizarea a 2 modele in vivo pentru evaluarea efectelor nutraceutice ale consumului de Zonar asupra carcinomului Walker 256 și ascitei Ehrlich
(modele înlocuite cu carcinomul de colon C26 și melanomul B16 inoculate subcutanat la șoareci din liniile BALB/c și C57Bl6).
În vederea atingerii acestor obiective au fost realizate activități specifice de către fiecare din partenerii responsabili de implementarea proiectului.
Activitățile desfășurate de PP1 au constat în: determinarea și caracterizarea proprietăților fizico-chimice ale Zonarului și produselor pe bază de Zonar
luate în studiu, prin utilizarea unor metode clasice standardizate; efectuarea unor determinări cantitative și calitative cu privire la proteinele
și peptidele bioactive care intră în compoziția produselor funcționale investigate, și care se află la originea proprietăților nutraceutice funcționale ale
Zonarului și produselor obținute pe bază de Zonar. Rezultatele obținute de PP1 au fost valorificate prin participarea cu 3 Postere la
2 manifestări științifice internaționale, prilej cu care 1 poster a fost recompensat cu Diploma de excelență pentru calitatea cercetărilor
efectuate și a rezultatelor prezentate. De asemenea, rezultatele obținute de PP1 au făcut obiectul a 2 articole originale acceptate pentru publicare
în reviste indexate Web of Science și 1 articol care a fost trimis pentru publicare la Journal of Food Science (IF-1.815).
Activitățile de cercetare desfășurate de coordonatorul proiectului (CO) au constat în: dezvoltarea și implementarea unui model de studiu a efectelor
funcționale nutraceutice ale Zonarului (și concentratului proteic obținut prin liofilizare din Zonar) în Diabetul zaharat de tip II indus experimental
la șobolani Wistar prin administrare de nicotinamidă și streptozotocină; studiul efectelor nutraceutice bioactive ale Zonarului și concentratului
proteic obținut prin liofilizare din Zonar asupra carcinomului de colon C26 și a melanomului B16 inoculate subcutanat la șoareci din liniile
BALB/c și C57Bl6. Rezultatele obținute de CO au fost valorificate prin participarea cu 2 Postere la National Conference of the Romanian Society of
Pathophysiology (cu participare internațională), prilej cu care Directorul de proiect a organizat și moderat o masă rotundă cu tema
Functional Foods as tools of the Alternative Medicine, în cadrul căreia a susținut o prezentare orală cu titlul
“Using nutraceutical foods as palliative and curative tools in the alternative medicine”. Promovarea obiectivelor și activităților specifice proiectului
a fost realizată și prin Workshop-ul cu titlul Bioetica Experimentelor pe Animale, organizat și moderat de Directorul de proiect în cadrul
Congresului XII Național de Medicină Veterinară, desfășurat la USAMV Cluj-Napoca în perioada 20-23 Septembrie 2017.
O parte din rezultatele obținute pe modelele experimentale investigate au fost valorificate prin elaborarea a 2 articole originale care au fost
acceptate pentru publicare în numărul 1 din 2018 al Romanian Rewiev of Veterinary Medicine, iar alte 2 articole sunt în lucru pentru a fi prezentate
în cadrul the 4th International Conference on Biomedical Polymers & Polymeric Biomaterials, 15-18 July 2018, Kraków, Poland (1) și publicate în
Journal of Diabetes Research (1). Mai trebuie menționate ca rezultate obținute pe parcursul implementării acestei etape și publicarea a
3 capitole într-o carte de specialitate elaborată de un colectiv international, sub redacția Prof. Ioan Marcus, PhD (Fiziopatologie:
Tulburări Funcționale și Mecanisme Etiopatogenice, Editura Roprint, Cluj-Napoca, 2017, 1000 pg. ISBN 978-973-53-1718-8).
Pe lângă toate acestea, au fost realizate și acțiuni de formare și dezvoltare a competențelor de conceperea și elaborarea unui proiect de cercetare,
precum și participări la evenimente naționale/internaționale în vederea dezvoltării unor noi parteneriate științifice în domeniul proiectului.
Pe parcursul acestei etape au avut loc mai multe întâlniri ale echipelor de cercetare, atât la sediul CO și PP1, cât și la sediul PP2
(SC. Embryom Capital Investment SRL Satu-Mare), ocazie cu care s-a elaborat și discutat planul de implementare a proiectului,
și respectiv managementul activităților și rezultatelor preconizate, inclusiv acțiuni de instruire a doctoranzilor în procesul tehnologic de fabricare a
Zonarului și a produselor pe bază de Zonar. Nu în ultimul rând, au fost proiectate și dezvoltate materiale de promovare a obiectivelor,
activităților și rezultatelor proiectului, respectiv a fost actualizată cu aspecte noi privind activitățile desfășurate pagina de Web a proiectului
(http://www.usamvcluj.ro/profi-zonar).
Descrierea științifică și tehnică, cu punerea în evidență a rezultatelor etapei și gradul de realizare a obiectivelor
(se vor indica rezultatele obținute și modul de diseminare a acestora)
Obiectivul 1: Determinarea compoziției chimice a Zonarului utilizând metode standardizate clasice;
Primul din obiectivele etapei II/2017 l-a constituit determinarea compoziției chimice a Zonarului și a produselor obținute din Zonar prin utilizarea unor metode clasice standardizate (descrise în detaliu în Anexa 1) de către PP1. Rezultatele obținute au fost furnizate sub forma unor Buletine de analiză, care sunt incluse în Anexa 2. Au fost determinate valorile cantitative ale mai multor produse pe bază de lactoser Zonar de către SC. Embryom Capital Investment SRL: Zonar (Z), Zonar cu ghimbir și miere (Z-GE-H), Zonar cu extract de cacao și miere (Z-CE-H), Zonar cu argint colloidal (Z-CS) și respectiv Zonarul Baby (Z-Baby).
Determinarea caracteristicilor fizico-chimice ale produselor pe bază de Zonar investigate
| Caracteristici | Zonar | Z-GE-H | Z-CE-H | Z-CS | M-W | Z-Baby |
|---|---|---|---|---|---|---|
| pH | 6,2 | 6,1 | 6,2 | 6,3 | 6.2-6.4 | 6,2 |
| Aciditate [°T] | 9 | 10 | 10 | 9 | 4 [SH]* | 9 |
| Substanță uscată [%] | 6.3 | 6.1 | 6.1 | 6.2 | 6-6.5 | 6.6 |
| Apă [%] | 93.7 | 93.9 | 93.9 | 93.8 | 93-94 | 93.4 |
| NaCl [%] | 0.2 | 0.19 | 0.19 | 0.19 | - | 0.3 |
| Lactoză [%] | 4.8 | 4.7 | 4.7 | 4.6 | 4.5-5 | 5.39 |
Legendă: M-W se referă la caracteristicile lactoserului prezentate în datele din literatură; Z este lactoserul Zonar, Z-GE-H este lactoserul Zonar cu extract de ghimbir și miere; Z-CE-H este lactoserul Zonar cu extract de cacao și miere; Z-CS este lactoserul Zonar cu soluție de argint colloidal; Z-Baby, toate fiind produse de PP3.
În Anexa 3.2 sunt prezentate concentraţiile mineralelor și oligoelementelor identificate in produsele testate. Pentru a se obține o formulă stabilă pornind de la proprietățile de bază ale zerului și pentru a le îmbunătăți, s-a încercat reducerea conținutului de sare din Zonar. De asemenea, substanțele minerale din concentrat, în special sărurile de calciu, măresc flocularea proteinelor serice din concentrat la încălzire, în timp ce anionii citrat și fosfat protejează Ca2+, crescând stabilitatea termică a proteinelor la un pH neutru.
Determinarea conţinutului de metale (Cu, Fe, Zn, Pb) este utilă în evaluarea calității lactoserului, în cursul tratamentului acestuia. Se poate stabili indirect şi o relaţie între distribuția metalelor minore și a urmelor acestora din lapte cu hrana animalelor şi cu condiţiile de mediu. Compoziția minerală diferă cel mai mult în funcție de pH și de cantitatea de acid lactic între diferitele tipuri de zer. La pH 6,0 sau mai mare o mare parte din continutul de Ca++ din lapte este reținut în brânză. Conținutul ridicat de Ca++ din Zonar pare să fie explicația pentru variațiile proprietăților fizico-chimice ale acestui produs, inclusiv în cee ace privește stabilitatea substanțial mai redusă, comparativ cu cea a zerului dulce. Datorită faptului că compoziția zerului demineralizat seamănă mult cu cea a laptelui matern, aproximativ 65% din cantitatea totală a zerului cu un continut redus de minerale este utilizată pentru fabricarea formulelor pentru sugari.
Obiectivul 2: Implementarea unui model in vivo pentru studiul efectelor funcționale nutraceutice ale Zonarului într-un model experimental de Diabet zaharat realizat pe șobolani Wistar;
Scopul obiectivului 2 l-a constituit investigarea efectelor nutraceutice funcționale ale Zonarului și concentratului proteic obținut din Zonar (CpZ) prin liofilizare pe model de Diabet zaharat tip II (DZ II) indus experimental la șobolani Wistar prin administrare de Streptozotocin și Nicotinamidă. În Anexa 4.1 sunt prezentate în detaliu aspectele tehnice privitoare la descrierea protocolului experimental, metoda de inducere a diabetului zaharat și metodele de investigație care au fost utilizate pentru evaluarea efectelor nutraceutice ale Zonarului și CpZ asupra animalelor cu DZ II. Inducerea DZ II la șobolani Wistar s-a făcut conform metodologiei descrise în literatura de specialitate (Islam și col., 2009; 2012), iar administrarea Zonarului și a CpZ s-a făcut în concordanță cu informațiile prezentate pentru alte studii efectuate pe sortimente de lactoser, respectiv de concentrate proteice obținute din zer (Bounous, 2000; Krissansen, 2007). Pe parcursul studiului au fost evaluate periodic aspecte privind starea generală a animalelor, evoluția greutății corporale, comportamentul alimentar al animalelor cu DZ, valorile glicemiei și alte particularități clinice relevante pentru aprecierea efectelor funcționale ale produselor studiate. Experimentul a durat 5 săptămâni, iar la sfârșitul studiului animalele au fost sacrificate sub narcoză cu eter, fiind prelevate probe de sânge și plasmă, respectiv de țesut pentru examenul histopatologic. Rezultatele au foost procesate statistic (cf. Anexa 4.1). Realizarea experimentului a fost aprobată de Comisia de Bioetică a USAMV Cluj-Napoca (Decizia Nr. 49/28.02.2017), iar proiectul a fost autorizat de DSVSA Cluj (Autorizație Nr. 49/30.03.2017).
Studiul a evidențiat următoarele aspecte majore: animalele din loturile experimentale au consumat zonarul și produsul obținut din zonar prin liofilizare în cantități care oscilau de la 25 la 75 ml/lot/zi, fără să manifeste reacții adverse sau semne digestive de intoleranță. Starea generală a animalelor s-a menținut s-a menținut bună pe toată durata experimentului, creșterea în greutate a fost constantă la toate loturile care au consumat Z și CpZ, comparativ cu lotul 4 (Diabet control), în cazul căruia scăderea în greutate a fost severă și progresivă, începând din ziua 0 până în ziua 35. Comparativ cu lotul martor de control (L1) care a primit furaj granulat și apă ad libitum, creșteriile în greutate la celelate loturi au fost mai puțin pronunțate, dat fiind faptul că aceste loturi au primit o cantitate fixă de furaj/zi (10/animal/zi). Rezultatele obținute la determinarea în dinamică a glicemiei și interpretarea lor sunt prezentate în Anexa 4.3. S-au notat valori mai reduse ale glicemiei la loturile DZ-Z (284.80 ± 83.16 mg/dl) și CpZ-Z, comparativ cu lotul 4 (449.60 ± 42.18 mg/dl), fapt ce susține un posibil efect protector al acestor produse. Valorile parametrilor hematologici (WBC, RBC) se încadrează în limite normale la loturile martor (Anexa 4.4) , inclusiv la loturile 5 (DZ-Z) și 6 (DZ-CpZ), comparativ cu lotul cu DZ (4) la care valorile sunt mai mici pentru toți parametri (WBC=6,44±2.01x103; RBC=7.63±1.53x106, comparativ cu WBC=8.99±2.01x103 și RBC=8.70±1.63x106 la lotul martor). Valorile insulinemiei și Hb. glicate (Anexa 4.5), sunt considerate markeri biochimici pentru severitatea evoluției DZ. Insulina este semnificativ statistic scăzută la lotul 4 (1.27±0.99mU/L) față de loturile 1 (15.10±2.89 mU/L), l2 (13.15±3.74mU/L) și 3 (15.39±3.6mU/L), în timp ce la loturile 5 și 6 se constată diferențe pozitive de +255.75% și +430.92% față de martorul diabetic. Diferențe semnificative în favoarea loturilor tratate cu Zonar și CpZ se constată și în cazul determinării ASAT, ALAT și PAL (Anexa 4.6), în special cu privire la valoarea PAL, care la lotul 4 este mai crescută cu 96,6% față de lotul martor, iar la loturile 5 și 6 scade cu -50,21% și -42,46% față de lotul 4 (772,53U/L). Determinarea trigliceridelor, colesterolului și HDL (Anexa 4.7) evidențiază valori normale pentru loturile de control (1,2,3) și diferențe procentuale pozitive pentru lotul cu DZ (+46,43%; +13,99% și +41,71%).
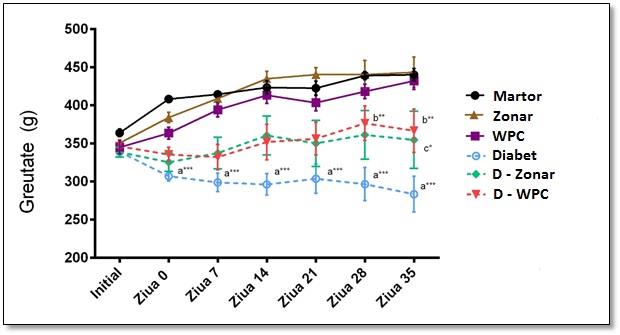
Fig. 1 Efectele Zonarului și a zonarului liofilizat (WPC) asupra greutății corporale la loturile experimentale
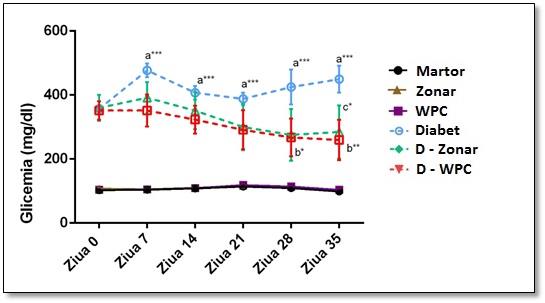
Fig. 2 Influența Zonarului și a Zonarului liofilizat (WPC) asupra glicemiei la loturile experimentale.
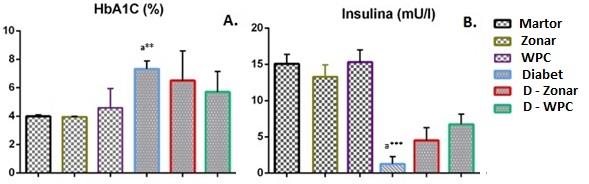
Fig. 3 Efectul Zonarului și zonarului liofilizat (WPC) asupra insulinemiei și hemoglobinei glicate.
Numeroase studii realizate în ultimii ani au semnalat efectele benefice pe care proteinele din zer le produc asupra homeostaziei glicemice, stimulând prin intermediul peptidelor bioactive secreția unor hormoni intestinali care determină efecte insulinotropice (Jakubowicz și col, 2013; Mignone și col., 2015). Mecanismele prin care proteinele din lactoser stimulează secreția de insulină nu sunt pe deplin cunoscute, fiind propuse mai multe explicații. Unul din aceste mecanisme face referire la acțiunea directă pe care o au aminoacizii cu catenă ramificată asupra secreției de insulină (Salehi și col., 2012). Dintre aceștia, leucina, izoleucina, valina, lizina și treonina par să fie responsabili de creșterea concentrației plasmatice de insulină. De asemenea, incretinele (ex: GIP, GLP-1) intestinale au fost citate ca fiind implicate în stimularea eliberării de insulină pancreatică, consecutiv ingestiei de lactoser (Jakubowicz și Froy, 2013).
Obiectivul 3: Determinări cantitative și calitative ale proteinelor și peptidelor bioactive din Zonar;
Determinarea proteinelor totale prin electroforeza
Proteinele din zer sunt reprezentate proteine majore și enzime minore cu actiune bacteriostatică, cum sunt lactoperoxidaza, lactoferina (sau lactotransferina capabilă să fixeze reversibil fierul și să-l neutralizeze, eliminand astfel toxicitatea lui avand si rol de ligant al Zn si Mg), lizozimul și alte produse de degradare derivate din caseină. Proteinele din zer și caseinele se deosebesc prin caracteristicile lor fizice și chimice, cum ar fi: proteinele din zer prezintă regiuni hidrofobe și hidrofile în timp ce caseina prezintă regiuni puternic hidrofobe; proteinele din zer sunt stabile în mediu slab acid, în timp ce cazeinele precipită în condiții acide și sunt insolubile la pH 4,6. Proteinele din zer au capacitate de legare a apei, această proprietate crescând prin denaturarea proteinei, fiind solubile la toate valorile pH-ului și insolubile la pH 5. Gelificarea are loc la 70°C (158°F) sau mai mare și este influențată de pH și de conținutul în săruri al produselor studiate. (Fig. 2, Anexa 4).
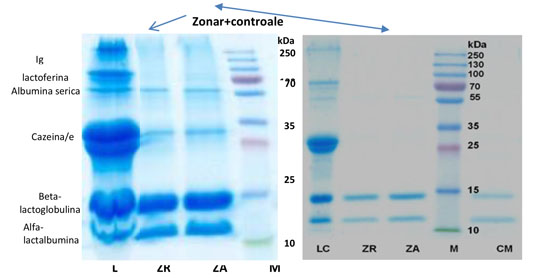
Fig. 4 Gelul SDS-PAGE a două probe de lactoser Zonar comparativ cu lapte comercial și cu zerul derivat din acesta prin precipitare simplă cu acid. ZA și ZR sunt 2 probe separate de lactoser Zonar; ZR este lactoserul inițial de lapte pentru a obține cele 3 băuturi cu ingrediente; LC este eșantionul de lapte comercial; CM este zer acid, preparat prin adăugarea de acid acetic la probele de lapte comercial; M - markeri ai greutății moleculare.
În Fig. 2 sunt ilustrate rezultatele SDS-PAGE privind Zonarul, comparativ cu laptele de vacă și cu zerul derivat printr-o procedură clasică (precipitare cu acid acetic). Proteinele majore identificate sunt, în conformitate cu studii anterioare privind alte preparate din zer, α-lactalbumină (14 kDa) și β-lactoglobulină (18 kDa). Acest profil este similar cu cel prezentat de o probă de zer de referință, preparată în laborator printr-un tratament chimic simplu. Față de aceste proteine, cantitățile de caseină (~30 kDa), albumină serică (66 kDa) sunt detectabile atunci când gelul este încărcat cu o cantitate mai mare de probă. În aceste condiții sunt prezente și semnale din regiunea 70+ kDA, care pot fi datorate lactoferinei (~ 76-80 kDa, în funcție de gradul de glicozilare) și imunoglobulinei (~70 kDa pentru peptida mare, 15 kDa pentru peptida mai mică).
| Proteinele totale din lactoserul Zonar prin electroforeza [μg/ml] ** | ||
|---|---|---|
| Centrifugat 15 min | Centrifugat 3-5 min | Necentrifugat |
| 538 μg/ml | 781 μg/ml | 2170 μg/ml |
Legenda: ** 0.6-0.65% pentru zerul dulce centrifugarea s-a efectuat pentru a îndepărta materiile solide în suspensie (proteine, celule). Proteinele totale obtinute prin electroforeza sunt de 538 μg/ml dupa 15 de centrifugare.
Proteinele bioactive din Zonar sunt un amestec de mai multe peptide (majore/minore), dintre care mai importante sunt β-lactoglobulină, α-lactoalbumină, imunoglobuline, Albumina serică bovină. Datorită complexității componentelor proteice și concentrațiile fiecărei proteine, excitația și maximul lungimii de undă de emisie a proteinei din zer variază de la 280 la 295 nm și, respectiv de la 330 nm la 350 nm. In figura 2 a) este ilustrată în grame, cantitatea de precipitat obtinut după centrifugare, iar în fig. 2b) sunt ilustrate spectrele UV vis masurate prin diluarea a 100 μL supernantant (proteina solubila) + 900 μl tampon fosfat 50 mM la pH 7.8 si 150 mM NaCl. Maximul de la 280 nm este prezent în toate probele și, deoarece ele au compoziții chimice similare, oferă o măsură imediată și precisă a conținutului relativ de proteină din fiecare probă. Au fost determinate proteinele totale prin metoda de electroforeză descrisă în Anexa 1. Profilul proteinelor este similar cu cel al zerului obținut din lapte comercial (vezi și tabel 2).
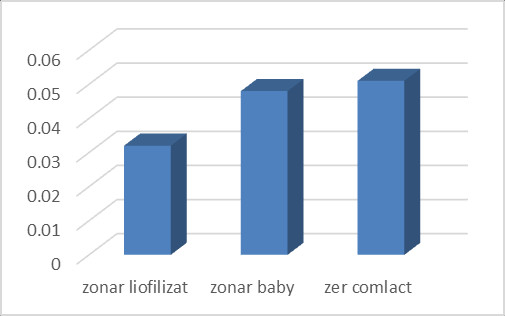
Fig. 5a Precipitat in grame (g) obtinut dupa centrifugare 5 min 14000 rpm;
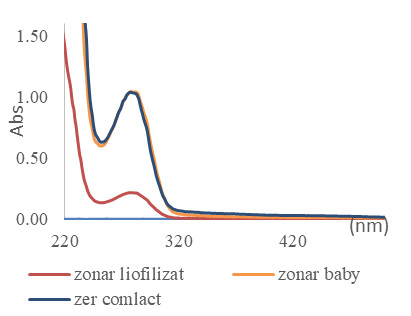
Fig. 5b Spectrele UV-vis ale supernatantului (după centrifugare 10 min la 14000 rpm)
| Atribuire posibila | M (kDa) | Rf | Zonar liofilizat (1)a | Zonar baby (5) | Zer comlact (6) | |||
|---|---|---|---|---|---|---|---|---|
| Materiale insolubile | - | >0.1 | 37.66 | 26.90 | 26.90 | 32.28 | 48.42 | 37.66 |
| - | 0.28-0.32 | - | - | - | 64.56 | - | 80.70 | |
| Lactoferina | 78 | 0.33-0.34 | - | - | - | - | - | - |
| Imunoglobuline | 70 | 0.35-0.38 | 107.60 | 102.22 | - | - | 96.84 | 91.46 |
| Albumina serică | 66 | 0.40-0.45 | 96,84 | 96,84 | - | - | - | - |
| - | 0.55 | - | - | - | - | - | - | |
| - | 0.61 | - | - | - | - | - | - | |
| Cazeina | 30 | 0.65-0.69 | - | - | - | - | - | - |
| β-lactoglobulina | 18 | 0.82-0.84 | 199.06 | 182.92 | 301.28 | 338.94 | 225.96 | 188.30 |
| α-lactalbumina | 14 | 0.86-0.89 | 96.84 | 129.12 | 134.50 | 102.22 | 166.78 | 139.88 |
| Total | 538 | 538 | 462.68 | 538 | 538 | 538 | ||
Legenda: a pentru fiecare produs s-au rulat două probe la grade de încărcare (concentrații) diferite.
Din analiza rezultatelor obținute rezultă că lactalbumina reprezintă 20-30% în toate probele, lactoglobulina reprezintă 35-45% cu excepția a Zonar-baby (unde urcă la cca 60%)., iar componentele cu masă moleculară de 60-80 kDa (lactoferina, imunoglobulina, BSA) reprezintă 15-30% din fiecare probă.
Analiza HPLC-UV a proteinelor bioactive din probele de lactoser
Continutul de proteine totale identificate prin HPLC variază pentru cele 10 probe de Zonar studiate, de la 2,25 g/l pentru Z01 la 1.57 la Zonar –Z10. Cea mai mare valoare s-a obtinut la produsul Zonar cu cacao de 2,616 g/l. Predominanta este cantitatea de α-lactalbumina în probele investigate (vezi Anexa 5 pentru detalii privind valorile obținute).
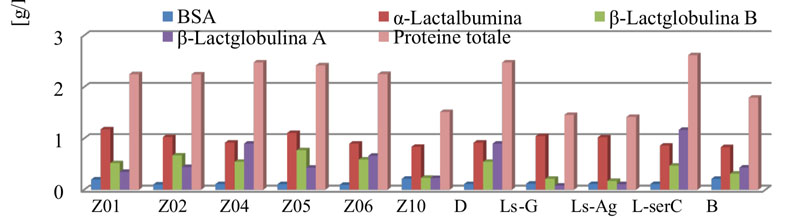
Fig. 6 Conținutul de proteine totale din produsele pe bază de zonar analizate prin HPLC
In Fig. 3 este ilustrat continutul de proteine totale din produsele analizate prin HPLC-UV, iar in Fig. 4 sunt prezentate cromatrogramele HPLC standard si a produsului Zonar. Au fost analizate 6 loturi de Zonar și produse pe bază de Zonar (ex: Z-Daily, Z cu argint, Z cu cacao, Zonar cu ghimbir și Z-Baby).
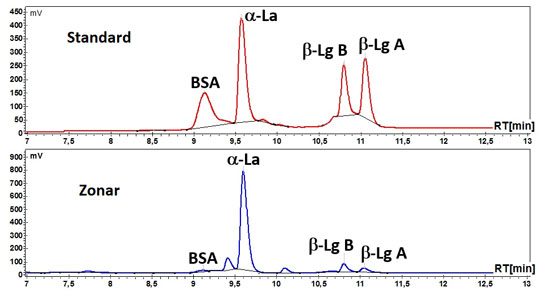
Fig. 7 Cromatogramele HPLC ale amestecului standard de proteine [BSA, α-lactalbumin (α-La), β-lactglobulin B (β-Lg B), β-lactglobulin A (β-Lg A)] și a proteinelor din lactoserul Zonar.
Determinarea lactozei prin cromatografia de lichid de înaltă performanță (HPLC)
Conținutul de lactoză a fost determinat prin HPLC-RI. Concentrația de lactoză variază de la 42,82 g/l (Zonar-Z06) la 53,49 g/l (Zonar-Z10), valorile fiind apropiate la Z02 (52.8 g/l), Z04 (52.93g/l) si Z10 (53.49 g/l).
Determinarea HPLC-UV a nitriților și nitraților din probele de lactoser
Nitriţii se elimină în cea mai mare parte prin zer, iar cantitatea rămasă în brânzeturi scade treptat în timpul procesului de maturare. Zonarul simplu are o concentrație de 11,58 mg/L nitrit de sodiu si 2,257 mg/L nitrat de sodiu. Nitratul de sodiu variază la Zonar si produsele studiate, fiind de 2.95 (Z-Baby) și 7,09 mg/L la Zonarul liofilizat.
| Probe Zonar | Nitrit de sodiu [mg/L] | Nitrat de sodiu [mg/L] |
|---|---|---|
| Zonar simplu (13.10.2017) | 11.58 | 2.257 |
| Zonar Baby (13.10.2017) | 14.76 | 2.95 |
| Zonar liofilizat [mg/g] | 116.66 | 7.09 |
Caracterizarea Zonar concentrat prin liofilizare
Dacă comparăm concentrațiile de Ca şi K din Zonar cu cele din zonarul liofilizat se observă valori mai mari de 10 ori pentru Ca și pentru K, iar în cazul Mg şi P valorile sunt mai mari de 11 ori. Concentraţia de Na din concentrat este mai mare de 4 ori faţă de Zonar., în timp ce pentru Zn, Fe şi Pb valorile au crescut de 5-7 ori faţa de cele din lactoserul lichid.
| Element [mg/kg] | Ca | K | Mg | Na | Cu | Fe | Pb | Zn | P |
|---|---|---|---|---|---|---|---|---|---|
| Lactoser | 305.61 | 751.86 | 67.45 | 104.79 | 0.909 | 2.485 | 0.019 | 0.630 | 418.395 |
| Zonar liofilizat | 3130 | 7870 | 800 | 451.44 | 0.9 | 16.99 | 0.15 | 3.24 | 4899 |
| Proteinele totale din lactoserul Zonar liofilizat prin analiza HPLC-UV [mg/g] | ||||
|---|---|---|---|---|
| BSA | α-lactalbumin | β-lactglobulin B | β-lactglobulin A | Total |
| 11.87 | 9.57 | 20.41 | 6.135 | 47.985 |
Determinarea aminoacizilor cu catenă ramificată din concentratele de proteine din lactoserul Zonar si Zonar Baby prin OPLC
Profilul aminoacizilor diferă între cazeinele și proteinele din zer, în sensul că cazeinele conțin o proporție mare de reziduuri de glutamină și prolină și proporții minore de arginină, în timp ce proteinele din zer conțin resturi de aminoacizi cu catenă ramificată (BCAA). BCAA sunt structuri chimice macromoleculare care includ o catenă laterală cu 1 atom de C și 3 atomi de hydrogen, fiind rerezentați de 3 din cei 9 aminoacizi esențiali, respectiv leucina (Leu), izoleucina (ILeu) și valina (Val), cu rol bioactiv important.
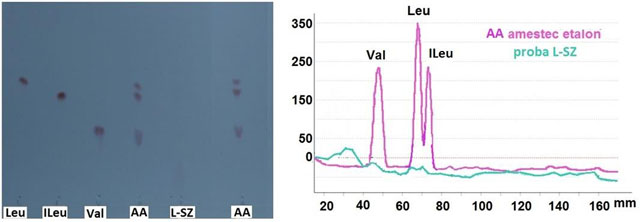
Fig. 8 Placa TLC si densitograma Zonarului concentrat si a etaloanelor de aminoacizi investigați.
Determinarea temperaturii de denaturare a proteinelor din Zonarul liofilizat, prin DSC
Termogramele corespunzatoare esantioanelor studiate prezintă aceeasi alură cu 3 peak-uri endoterme. Din figura 11 (Anexa 10) se observă ca lactoserul Zonar prezinta endoterma de tranziție la 80,530C, Zonarul Baby la 73,3 oC, iar zerul comercial la 75,34 oC. Din datele din literatura, comportamentului termic al proteinelor majore din zer a fost investigat prin DSC până la 1500C si au fost observate două efecte distincte de căldură: până aproape de 700C efectul este atribuit denaturării, iar aproape de 1300C este atribuit denaturarii structurii proteice rămase. Referitor la a doua endoterma de tranzitie, aceasta se poate atribui la peste 1000C, β-lg si ruperii legaturilor disulfidice, care au un rol foarte important în stabilizarea arhitecturii spaţiale a moleculei proteice, urmata de denaturarea proteinei. Din figura 11 (Anexa 10) se poate observa a 2-a izotermă de tranzitie în cazul esantionului Zonar care prezinta o temperatura a peak- ului (Tp) de 144.230C, în cazul esantionului Z-Baby temp. de 138,520C, iar in cazul zerului comercial temperatura este de 139,170C. Lactoserul Zonar este mai rezistent la denaturare cu 5,710C față de Zonarul-Baby si cu 5,060 C fata de lactoserul commercial. Concluzia este ca lactoserul Zonar conține proteine mult mai rezistente la denaturare decât celelalte două eșantioane din produsele investigate. Pentru un raport mai mare de β-lg/α crește temperatura de denaturare, fapt care ar putea fi explicat printr- o denaturare superioară caracteristică pentru β-lg pură. Această creștere este mai pronunțată atunci când concentrația proteinei este mai mică, probabil datorită cantității mai mici de proteină care se denaturează.
Testarea activității antibacteriene a zerului și a proteinelor concentrate din zer
Capacitatea antimicrobiană a zonarului sau a proteinelor din lactoseruri a fost evaluată prin testarea susceptibilității difuzimetrice (metoda rondelelor). Au fost testate 3 tipuri de lactoser sub forma lichidă si Zonar liofilizat. Microorganismele test utilizate în acest studiu au fost: E. coli ATCC 25922 și Staphylococcus aureus ATCC 25923 din colecția Laboratorului de Microbiologie, Facultatea de Biologie și Geologie, UBB Cluj. După 24 de ore de incubare la 37 °C s-a măsurat diametrul de inhibiție pentru fiecare tip în parte. S-a observat că după incubare au apărut zone de inhibiție. La tulpina Gram pozitivă (S. aureus) toate cele 3 zeruri testate au prezentat zone de inhibiție mai mari ca la tulpina Gram-negativă (E. coli). (Anexa 8 RIA)
| Notare probe | Proba | Diamentrul zonei de inhibitie (mm) | |
|---|---|---|---|
| Staphylococcus aureus | Escherichia coli | ||
| 1 | Zonar liofilizat | 5 | 20 |
| 2 | Zonar Baby | 9 | 8 |
| 3 | Zonar lactoser | 10 | 8 |
| 4 | Zer Comlact | 9 | 8 |
Investigarea structurii suprafeței pulberilor din zerul liofilizat prin metoda SEM
Pentru analiza suprafeței probelor a fost utilizat un microscop INSPECT S (FEI Co). Prin analiza microscopiei electronice de scanare, este prezentata, la o magnitudine de x 1000 si respectiv x 5000, structura pulberii obtinuta prin liofilizare din lactoserul Zonar. Din imaginea SEM se observă structura suprafeței pulberii, cu aglomerări de particule de diferite forme. La o mărire mai mare (x 5000) se observă o structură încrețită a suprafețelor eșantionului cu particule de 1-10 μm, mai mult sau mai puțin rotunjite (Anexa 11).
Obiectivul 3: Dezvoltarea a două modele in vivo pentru evaluarea efectelor clinice și paraclinice ale consumului de Zonar asupra dezvoltării carcinomului Walker 256 și Ascitei Ehrlich
Pentru realizarea obiectivului 4 au fost utilizate 2 modele de studiu in vivo a efectelor nutraceutice ale Zonarului pe șoareci inoculați subcutanat cu celule de carcinom C25, și respectiv cu melanomul B16. Am utilizat aceste sisteme tumorale întrucât grefele efectuate din carcinomul Walker 256 la șobolani Wistar nu s-au devoltat la animalele gazdă, foarte probabil datoritpă contaminării țesutului tumoral sau ca urmare a unor incompatibilități antigenice. Carcinomul de colon C26 inoculat la șoareci BALB/c și melanomul B16 inoculat la șoareci C57BL6 sunt sisteme tumorale de transplant mult mai stabile, mai ușor de manipulat și mai responsive la variabilele experimentale cu potențial terapeutic, motiv pentru care am decis utilizarea lor în acest studiu. Metodologia de preparare, conservare și inoculare a celulelor tumorale de C26 și B16, precum și protocolul experimental utilizat sunt prezentate în detaliu în Anexa 5.1 și Anexa 6.1. Pentru fiecare model experimental s-au utilizat 6 loturi de animale tineret (masculi și femele) (șoareci BALB/c pentru C26 și șoareci C57BL6 pentru B16), a câte 5 animale/lot. Animalele au fost supuse dietei cu Zonar și Zonar liofilizat începând cu ziua 7 de la inocularea celulelor de C26 și de B16. Pentru testarea efectelor biologice ale produselor studiate s-a realizat o dietă bazată pe Zonar/CpZ și hrană standard, fiind calculat necesarul zilnic de calorii pentru un animal de 25 g. Nutrețul standard are 3.63 kcal/g conform Anexei.5.1, 10 ml de Zonar are 2.35 kcal și 1 g de Zonar liofilizat (CpZ) are 4.13 kcal, conform analizelor effectuate de PP1. Necesarul caloric bazal al unui animal adult este de 160kcal/kg/zi sau 670kJ/kg/zi, iar în cazul acestui studiu s-a calculat un necesar caloric bazal respectând standardele publicate de National Research Council (US) Subcommittee on Laboratory Animal Nutrition, 1995. Mâncarea standard a fost administrată 1/zi (15 g furaj granulat/lot), iar Zonarul și CpZ au fost administrate de 2 ori/zi, timp de 14 zile, în cantitate de 10 ml/animal și 1g CpZ/lot diluat în 10 ml Zonar. Experimentele au durat 28 de zile, timp în care s-a înregistrat evoluția greutății corporale (g/animal/lot) și rata creșterii tumorale (volumul tumoral). Greutatea animalelor a fost măsurată săptămânal pe toată durata experimentului. Tumorile subcutanate au fost măsurate la 7, 14, 21 și 28 de zile, iar volumul tumoral a fost calculat după formula: V= 0.52 x a2 x b (a-diametru mic, iar b- diametrul mare exprimat în mm3). La sfârșitul experimentului animalele au fost sacrificate prin dislocare cervicală sub narcoză cu Isofluran. Au fost măsurate volumul și greutatea tumorilor, determinându-se astfel greutatea carcasei animalului. Totodată s-au recoltat probe de sânge și țesut (ex: splina și ficatul) în vederea examenului histopatologic. Experimentele au fost aprobate de Comisia de Bioetică a USAMV Cluj-Napoca (Decizia Nr. 48/28.02.2017), iar proiectul a fost autorizat de DSVSA Cluj (Autorizație Nr. 49/30.03.2017).
Interpretare rezultate experiment C26+Zonar/Zonar liofilizat
Nu s-au înregistrat diferențe semnificative statistic între loturile martor și cele cu dietă bazată pe Zonar. În ziua 21 s-a evidențiat o scădere a greutății corporale la loturile 4 (19±1.41 g/lot), 5 (18.6±2.5 g/lot) și 6 (16.6±2.07 g/lot) față de lotul martor (22.6±0.54 g/lot) (p≤0.001). Totodată, s-a înregistrat o scădere a masei corporale la toate loturile inoculate cu carcinom de colon (lot4: 19.4±1.34 g/lot, lot5: 18±2.82 g/lot , lot6: 16.6±2.07 g/lot) în comparație cu lotul martor (23±0.7 g/lot) (p≤0.001) și în ziua 28.
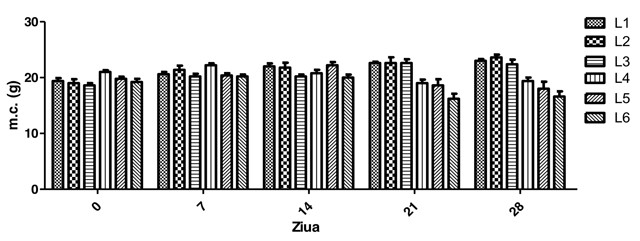
Fig. 9 Influența produlsului Zonar asupra dinamicii masei corporale la șoarecii inoculați cu linia tumroala C26 (Media ± Eroarea Standard a Mediei) (n = 5) (Anova two way, Bonferoni post test.
În cazul carcinomului C26 creșterea tumorală are loc în 2 faze (Aulino și col, 2010). Prima faza durează 14 zile de la inoculare și este caracterizată printr-o creștere tumorală lentă, după care urmează o fază de creștere tumorală rapida, cu tumori care ajung la o greutate de peste 2g și un volum mai mare de 200 mm3. În studiul de față dieta bazată pe consumul de Zonar și Zonar liofilizat are un efect vizibil anti- tumoral în ziua 28 în ceea ce privește reducerea volumului tumoral la lotul 5 (1.45±0.19 g/lot) și 6 (1.38±0.31 g/lot) față de lotul tumoral (2.32±0.56g/lot). S-a evidențiat astfel o scădere a greutății tumorale la lotul 5 (1.4±0.73 g/lot) și lotul 6 (1.42±0.24 g/lot) fațâ de lotul tumoral de control (1.66±0.29 g/lot).
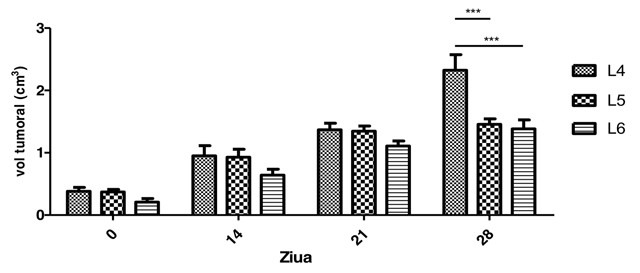
Fig. 10 Influența Zonarului asupra dinamicii volumului tumoral la șoarecii inoculați cu C26 (Media ± Eroarea Standard) (n=5) (Anova two way, Bonferoni post test, *** p<0.001 comparativ lotul L4);
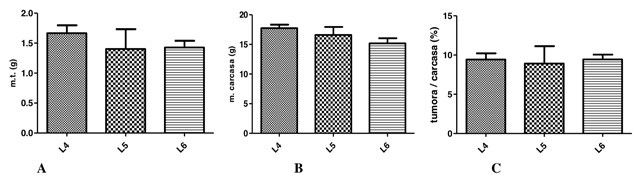
Fig. 11 Efectele Zonarului asupra masei tumorale (A) masei carcasei (B) (g) și asupra roportului greutate tumoră/greutate carcasă (C) la șoarecii inoculați cu celule de carcinom de colon C26 (Media ± Eroarea Standard a Mediei) (n = 5) (Anova one way, Dunnet post test, * p<0.05 comparativ lotul L4);
La lotul 6 (15.17±1.93 g/lot), lot hrănit cu Zonar și WPC s-a observant o scădere în greutatea carcasei față de lotul 4 (17.73±1.3 g/lot) sau controlul tumoral (p≤0.05). Nu s-au înregistrat diferențe semnificative statistic la calcularea valorii procentuale a masei tumorale raportată la greutatea carcasei animalelor cu tumori.
Examenul macroscopic al tumorilor a evidențiat diferențe evidente între loturile experimentale în ceea ce priveste dimensiunea si aspectul pe sectiune al tumorilor. Formatiunile tumorale recoltate de la animalele lotului martor au prezentat cea mai mare dimensiune si greutate, în timp ce tumorile provenite de la loturile tratate au avut dimensiuni mai mici si pe sectiune au prezentat multiple focare de necroză, închise la culoare, la animalele din lotul 6 notându-se cele mai întinse focare de necroza intratumorală.
La examenul histologic al țesutului tumoral prelevat de la lotul 4 am notat un carcinom anaplazic incapsulat, cu celularitate ridicată. Formatiunea tumorală este situată subcutanat si comprimă structurile tisulare adiacente, nu se extinde peste marginile de rezecție, având un diametru de 1.5 x 2cm, sunt bine delimitat, încapsulate, constituind o masa neoplazica solidă si expansivă. Tumorile sunt intens celularizate, alcătuite din celulele slab diferentiate (de origine epiteliala), în centrul tumorii observându-se multiple microfocare de necroza tumorala. Celulele tumorale sunt mari, de 35-50 μm in diametru, au forma rotunda sau ovala, cu margini indistincte, citoplasma fin granulara, eozinofilica, pe alocuri usor vacuolara si raport nucleu citoplasma în favoarea nucleului. Anizocitoza si anizocarioza sunt severe, evidente iar numeroase celule prezinta kariomegalie. Tumora este vascularizată moderat, fiind prezente rare capilare. Numeroase mitoze sunt observate pe toate sectiunile, indicele mitotic variind de la 5 la 10/camp micro- scopic (Ob 40x) cu numeroase mitoze atipice. Polimorfismul nuclear si celular este foarte accentuat.
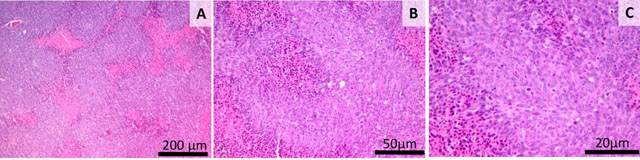
Fig. 13 Lotul 4 (martor C26). Masă tumorală solida, numeroase microfocare de necroza (A), celularitate ridicata, anaplazie marcanta, raport nucleu/citoplasma in fovoarea nucleului, indice mitotic crescut, microfocare de necroza si numeroase celule tumorale care sufera apoptoza (B,C), Colorația HE, Bară =200 μm (A), Bară =50 μm (B), Bară =20 μm (C).
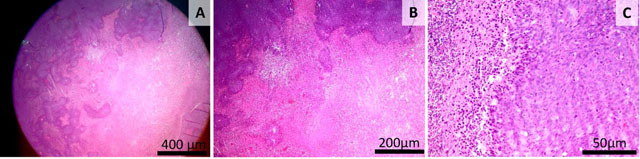
Fig. 13 Lotul 5 (C26+Zonar) Focare intinse de necroza intratumorala, cu prezenta unor resturi celulare eozinofilice si hemoragii intratumorale (A,B); interfata tumora, zona de necroza, celule inflamatorii mononucleare si rare neurofile (C), Colorația HE, Bară =400 μm (A), Bară =200 μm (B), Bară =50 μm (C).
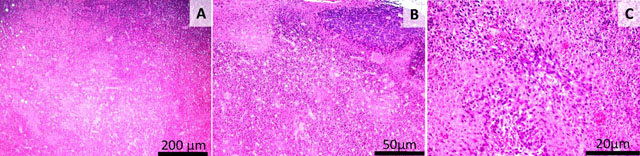
Fig. 14 Lotul 6 (C26+Zonar liofilizat). Necroza intratumorala masiva, cu prezenta unor resturi celulare eozinofilice (A,B,C); Rare celule tumorale viabile la periferia formatiunii (A,B), Necroza masiva, hemoragii (C) Colorația HE, Bară =200 μm (A), Bară =50 μm (B), Bară =20 μm (C).
Concluzii
Efectul antiproliferativ cel mai pronunțat a fost observat în cazul Zonarului liofilizat, fapt demonstrat de marirea ariilor de necroză și creșterii vascularizației la acest lot de animale.
Interpretare rezultate experiment Melanom B16+Zonar/Zonar liofilizat
Modelul de transplantare subcutanată (sc) a melanomului B16 este utilizat extensiv pentru studiul eficacității unor terapii antiproliferative. Celulele de melanom B16 grefate sc. formează o masă tumorală palpabilă în 5 până la 10 zile de la realizarea transplantului, care se va dezvolta până la dimensiuni de 1× 1×1 cm într-un interval de 14-21 de zile. După 21 zile de la transplantare tumorile se necrozează frecvent și încep să se ulcereze, fiind recomandată sacrificarea animalelor înainte de acest moment (Humane endpoint). Rata de proliferare tumorală a fost foarte accentuată, în special după ziua 7 de la transplant, la toate loturile inoculate cu B16. În ce privește evoluția greutății corporale, după ziua 21 s-a evidențiat o creștere semnificativă în greutate la loturile 4 (+29.4±4.27 g/lot), 5 (+30.4±2.88 g/lot) și 6 (+29.8±1.64 g/lot) față de lotul martor sănătos (22.2±1.3 g/lot) (p≤0.001). La sfârșitul experimentului lotul 3 (Zonar) înregistrează o creștere procentuală de 0.9% la 21 de zile și 2.61% la 28 de zile față de martor, iar la lotul 3 se constată o scădere procentuală a Gc. față de loturile 1 și 2 pe toată perioada studiului (Fig. 15). La lotul 4 (B16) s-a înregistrat o creștere a masei corporale, evidentă din ziua 21 (+32.43%) și ziua 28 (+20%). Lotul 5 (C26+Zonar) înregistrează o creștere a greutății corporale față de lotul 2 (martor Zonar), probabil datorită datorită dezvoltării tumorale expansive, diferența procentuală fiind de +37.71% în ziua 21. Față de lotul 4 (B16) se înregistrează o scădere a greutății corporale în ziua 28, diferența procentuală fiind însă nesemnificativă (-0,72%). La lotul 6 s-a înregistrat de asemenea o diferență pozitivă față de lotul iar față de lotul 4 se constată o diferență % similară, fiind mai evidentă în ziua 14 (+9.65%) (Fig.15).
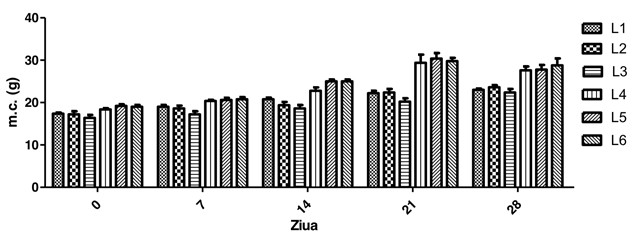
Fig. 15 Influența produlsului Zonar asupra dinamicii masei corporale la șoarecii inoculați cu melanomul B16 (Media ± Eroarea Standard a Mediei) (n = 5) (Anova two way, Bonferoni post test)
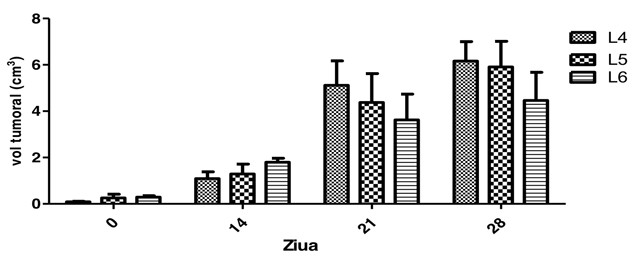
Fig. 16 Influența consumului de Zonar și Zonar liofilizat asupra dinamicii volumului tumoral la șoarecii C57BL6 inoculați cu B16 (Media ± Eroarea Standard a Mediei) (n=5) (Anova two way, Bonferoni post test, *** p<0.001 comparativ lotul L4). Se constată o scădere a greutății tumorilor la lotul 5 (7.09±3.34 g/lot) și lotul 6 (6.39±3.64 g/lot) comparativ cu lotul tumoral de control (7.97±2.2 g/lot).
Volumul tumoral a înregistrat la lotul 5 (B16+Z) o creștere procentuală în ziua 7 (+180.43%) și 14 (+18.35%) postinoculare prin comparație cu lotul 4. În schimb s-a produs o scădere a valorii diferențelor procentuale la același lot în ziua 21 (-14.48%) și 28 (-4.22%) față de volumul tumoral al lotului 4, scădere care ar putea fi determinată de consumul produselor pe bază de Zonar. Asemănător lotului 5, la lotul 6 s-a înregistrat o scădere procentuală față de lotul 4 în ziua 21 (- 29.16%) și ziua 28 (- 27.6%). Diferențele procentuale care marchează volumul tumoral la lotul 6 prin comparație cu lotul 5 se caracterizează de asemenea prin valori negative în a doua parte a experimentului (Ziua 21=17.16% și ziua 28=-24.41%).
Explicația acestor diferențe ar putea fi dată de aportul crescut de proteine bioactive și aminoacizi esențiali (ex: leucină, cisteină, izoleucină, arginină, metionină, valină etc), cunoscuți ca fiind responsabili de consolidarea sistemelor antioxidante celulare, ceea ce ar putea constitui un sprijin în confruntarea organismului animal cu creșterea tumorală malignă. Studii recente efectuate pe rozătoare indică faptul că proprietatea antitumorală a produselor pe bază de lactoser se datorează fracțiunilor proteice bioactive.
Cel mai studiat și cunoscut efect antiproliferativ este dat de formarea complexului α-lactalbumina bovină-acid oleic, care distruge celulele tumorale printr-un mecanism care implică permeabilizarea membranei lizozomale. De reținut că interacțiunea α-lactalbumina cu acidul oleic este stereospecifică, motiv pentru care acizii grași cis- nesaturați se leagă de α-lactalbumina, și doar acidul oleic interacționează cu α-lactalbumina într-o formă compactă, rezultând un efect antiproliferativ. Alfa- lactalbumina posedă proprietăți antiproliferative demonstrate asupra carcinomului de colon C26 grefat la șoareci C57Bl6, precum și asupra liniilor celulare obținute din C26 (Rodriguez și colab., 2009). La rândul ei, β-lactoglobulina asigură protecție împotriva dezvoltării tumorale când este administrată oral.
Mecanismul antitumoral se datorează conținutului ridicat în Aa care conțin sulf (ex: cisteina). Pe de altă parte, β-lactoglobulina influențează concentrația tisulară de tiol-glutation, o tripeptidă multifuncțională ce leagă și elimină mutagenii și/sau carcinogenii endogeni și exogeni. De asemenea, albumina serică bovină inhibă creșterea celulelor de carcinom mamar uman (linia MCF-7) dependent de concentrație, aceasta interferând cu proliferarea malignă prin modularea activității factorilor regulatori autocrini ai creșterii celulare/tisulare. Bounous și col., (1991) demonstrează că dietele pe bază de proteine din lactoser determină o creștere a concentrației glutationului seric, care este un factor critic în dezvoltarea răspunsului imunitar. Practic, proteinele bogate în cisteină reprezintă o rezervă importantă de aminoacizi cu sulf, necesari pentru aprovizionarea cu GSH în cursul elaborării răspunsului imun. Alte mecanisme biologice prin care proteinele funcționale din lactoser își exercită efectul antitumoral sunt reprezentate de activarea proteinei p53 în celulele modificate și de inhibiția neoangiogenezei (Bounous și col., 2003).
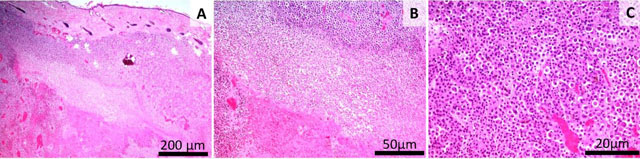
Fig. 17 Lotul 4. Masă tumorală infiltrativă, cu focar de necroza centrala (A), celularitate ridicata, anaplazie marcanta, focar de necroza intins, vase sanguine si infiltrate inflamator la periferia zonei de necroza (B), Numeroase celule anaplazice, rare vase de sange (C) Colorația HE, Bară =200 μm (A), Bară =50 μm (B), Bară =20 μm (C).
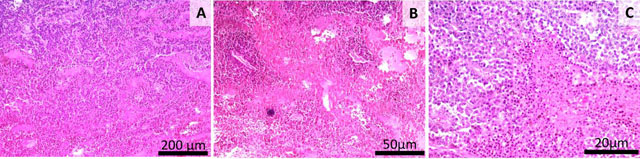
Fig. 18 Lotul 5 Numeroase focare de necroza in masa tumorala (A,B), celularitate ridicata, anaplazie marcanta, focar de necroza intratumorala (C) Colorația HE, Bară =200 μm (A), Bară =50 μm (B), Bară =20 μm (C).
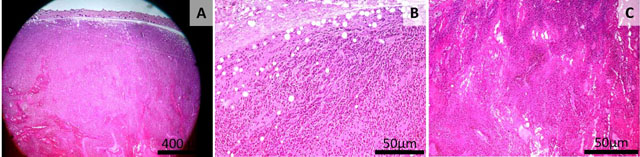
Fig. 19 Lotul 6. Masă tumorală bine delimitate, fara invazie dermica, focar intins de necroza (A), Material eozinofil care disocieaza celulele tumorale din regiunea subdermala, numeroase vacuole de lipide (B), Focar de necroză intratumorală, muneroase vase sanguine (C) Colorația HE, Bară =400 μm (A), Bară =50 μm (B,C).
Focarele necrotice intratumorale sunt multiple si de dimensiuni mai mari la lotul 5 decat la lotul 4, iar în focare au fost identificate numeroase resturi celulare cu aspect eozinofilic și fibrină. Infiltratul este discret, reprezentat de neutrofile degenerate si rare macrofage. In centrul focarelor necrotice se observa un material eozinofilic care disociaza fibrele de colagen si celulele tumorale (vezi Anexa 6.4).
Concluzii
Efectul antitumoral cel mai pronunțat s-a observat în cazul combinării Zonarului cu concentrat proteic obținut prin liofilizare, fapt demonstrat de extinderea ariilor de necroza tumorală si de cresterea vascularizatiei tumorale, respectiv de absența invaziei tumorale la nivel dermic la acest lot.